乙二醇
中医宝典 > 乙二醇
| 乙二醇 | |
|---|---|
 | |
 | |
| IUPAC名 Ethane-1,2-diol | |
| 别名 | 乙撑亚胺 MEG 1,2-乙二醇 |
| 识别 | |
| CAS号 | 107-21-1 |
| SMILES |
|
| 性质 | |
| 化学式 | C2H4(OH)2 |
| 摩尔质量 | 62.068 g·mol⁻¹ |
| 密度 | 1.1132 |
| 熔点 | −12.9 °C (8.8 °F) |
| 沸点 | 197.3 °C (387 °F) |
| 溶解性(水) | 与水以任意比互溶 |
| 危险性 | |
| 闪点 | 111 °C (closed cup) |
| 自燃温度 | 410 °C |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
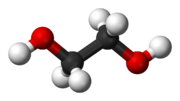
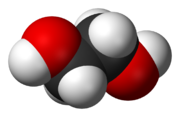
乙二醇,又名甘醇。化学式HOCH2—CH2OH。一种简单的二元醇。无色无臭、有甜味液体,能与水以任意比例混合。用作溶剂、防冻剂以及PET等的原料。
乙二醇对动物有毒性,人类致死剂量估计为1.6 g/kg,[1]不过成人服食30毫升已有可能引致死亡。[2]
目录 |
制备
乙二醇可由乙烯透过反应中间体环氧乙烷产生。环氧乙烷与水的反应产生乙二醇的化学反应式如下:
- C2H4O + H2O → HO–CH2CH2–OH
此反应可由酸或碱的催化下加速反应,或在中性pH值条件下提高的温度也可以加速反应。乙二醇最高的产率发生在酸性或中性pH下与大量过量的水,在这条件下,乙二醇的产量可达90%。主要的副产物是属于乙二醇低聚物的 二甘醇、三甘醇、四甘醇。每年生产约六十七亿公斤。 有一个选择性较高的方式是使用OMEGA process。反应式为:
- C2H4O + CO2 → C3H4O3
- C3H4O3 + H2O → HOC2H4OH + CO2
在OMEGA process中,第一步骤:环氧乙烷先与二氧化碳转变成碳酸乙烯酯(Ethylene carbonate)第二步骤:碳酸乙烯酯(Ethylene carbonate)与水反应,选择性地产生乙二醇单体。在第二步骤被释放的二氧化碳,可以回馈到第一步骤再使用。[3]
毒性
乙二醇的毒性不高,目前已知对人类的最低致死剂量LDLO为786毫克/公斤。[4]乙二醇最大的危险性在于它的甜味。因此相较于其他有毒物质,孩童和动物比较容易因摄取大量的乙二醇而中毒。经过消化系统作用,乙二醇会先被氧化成乙醇酸,再被氧化成草酸。草酸及其副产物会先影响中枢神经系统,接着是心脏,而后影响肾脏。如无适当治疗,摄取过量乙二醇会导致死亡。[5]
根据美国毒物管制中心2007年的资料,当年有大约1000起乙二醇中毒事件且其中有16人死亡。2008年则有7人死于乙二醇中毒。(Toxicity, Ethylene Glycol)
生活环境中的乙二醇
- 生活环境中的乙二醇主要来自于机场的用来除冰的除冰剂或其他含有乙二醇的产品。
- 乙二醇在大气中自然分解的时间大约为10天。
- 水中或土壤中的乙二醇则需大约几个星期才会分解。[6]
参考资料
- ↑ http://mtcc.vghtc.gov.tw/intrChemicalAidCont.asp?CasNo=107-21-1
- ↑ Field D. Acute ethylene glycol poisoning. Crit Care Med. 1985, 13 (10): 872-3. PMID 4028762.
- ↑ Siegfried Rebsdat; Dieter Mayer (2005), "Ethylene Glycol", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi: 10.1002/14356007.a10_101
- ↑ Safety Officer in Physical Chemistry. Safety (MSDS) data for ethylene glycol. Oxford University. November 23, 2009 [December 30, 2009].
- ↑ Ethylene glycol. National Institute for Occupational Safety and Health. Emergency Response Database. August 22, 2008. Retrieved December 31, 2008.
- ↑ (CDC ToxFAQs)
参考来源
6个分类: 无附加数据页的化学条目 | 空气污染物 | 家用化学品 | 醇类溶剂 | 二醇 | 二碳有机物
